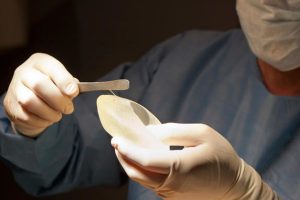
在監管機構提醒乳房植入物製造商Allergan公司使用該其產品會增加癌症風險後,該公司週三發佈一份針對某些紋理植入物的全球召回。
FDA稱,新資訊顯示Allergan的紋理表面Biocell乳房植入物與大多數罕見淋巴瘤病例有關,因此,它要求實施這一召回。此前,法國、澳大利亞和加拿大也採取了類似行動。
不過,FDA不建議已經植入的女性將其移除,因為這種癌症非常非常罕見。但是他們說,如果她們有包括疼痛和腫脹在內的症狀,就應該諮詢醫生。
Biocell植入物有紋理表面,旨在防止滑動和減少疤痕組織。它們只占美國市場的5%。在美國使用的大多數隆胸植入物表面光滑。
週三的召回不會影響Allergan光滑植入物,也不會影響以Microcell品牌出售的另一種Allergan紋理植入物。
2011年,健康當局首次將乳房植入物與癌症聯繫起來。這種疾病不是乳癌,而是生長在乳房周圍疤痕組織中的淋巴瘤。它生長緩慢,通常可以通過手術移除植入物來成功治療。
最近直到五月份,FDA還在表示這種危險並不意味著美國禁止使用紋理植入物。但FDA週三表示,新資料顯示Allergan植入物與癌症有直接聯繫,而其他紋理植入物則沒有。
FDA說,最新資料顯示,在全世界570例確認的淋巴瘤病例中,80%以上與Allergan植入物有關。監管機構估計,與在美國銷售的其他紋理植入物相比,使用Allergan植入物患此病的風險要高出6倍。
FDA官員說,他們在收到116份新癌症報告後決定採取行動。這些報告將與該疾病相關的死亡人數從9人增加到33人,其中至少有12名女性裝了Allergan乳房植入物。
FDA設備主管Jeffrey Shuren說,死亡人數增加對他們要求召回的決定起到了重要作用。
考慮到全球估計有1000萬女性進行了乳房植入,新數據仍然反映出這一疾病是極其罕見的。FDA估計數十萬美國女性有Biocell植入物。
關於這種疾病的確切發生率,即與乳房植入物相關的間變性大細胞淋巴瘤,尚無確切的一致意見。公佈的估計數從1/3000到1/30000不等。
Allergan在一份聲明中說,它將不再出售或分銷Biocell植入物和組織擴張器。該公司表示將指示外科醫生退回未使用的植入物。
每年大約有40萬美國女性進行乳房植入手術。這些植入物有一個矽膠外殼,填充鹽水或矽膠。矽膠填充的植入物在美國更受歡迎,因為它們被認為更自然。
在美國,Johnson & Johnson和Sientra也製造紋理乳房植入物。一個較小的製造商Ideal Implant只銷售光滑植入物。